Leuproreline-acetaatsuspensieis een injecteerbare suspensie met langdurige-werkende-afgifte, die zich onderscheidt door de nauwkeurig ontworpen suspensieformulering die het medicijn gelijkmatig verspreidt in een microdeeltjesdispersiesysteem. Het combineert de voordelen van stabiliteit en gerichte afgifte en biedt een zeer effectieve therapeutische oplossing voor geslachtshormoon-gerelateerde ziekten. Na intramusculaire injectie lossen de microdeeltjes langzaam op en geven het medicijn vrij op de injectieplaats, waardoor abrupte schommelingen in de medicijnconcentratie in het bloed worden vermeden. Deze formulering heeft een hoge biologische beschikbaarheid, ontgaat het first-effect van orale toediening en vereist een lage toedieningsfrequentie (eenmaal per maand), waardoor het geschikt is voor behandelingsbehoeften op de lange- termijn. Klinisch wordt het vaak gebruikt voor prostaatkanker, endometriose en andere aandoeningen. De suspensieformulering vermindert lokale irritatie en verbetert de tolerantie voor de patiënt, terwijl de snelheid van de geneesmiddelafgifte nauwkeurig wordt gecontroleerd om een stabiele werkzaamheid en medicatieveiligheid in evenwicht te brengen, waardoor het een onderscheidend preparaat op het gebied van endocriene therapie wordt.
Ons productenformulier


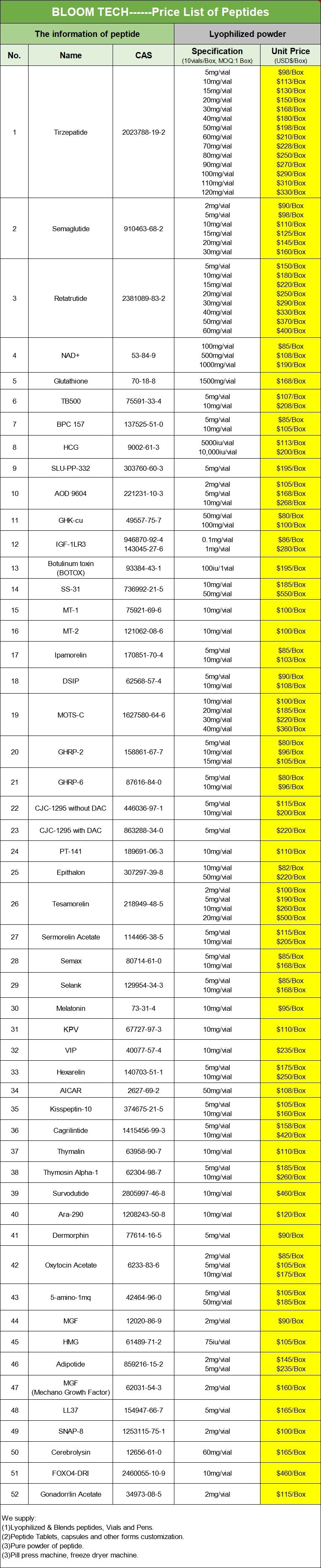
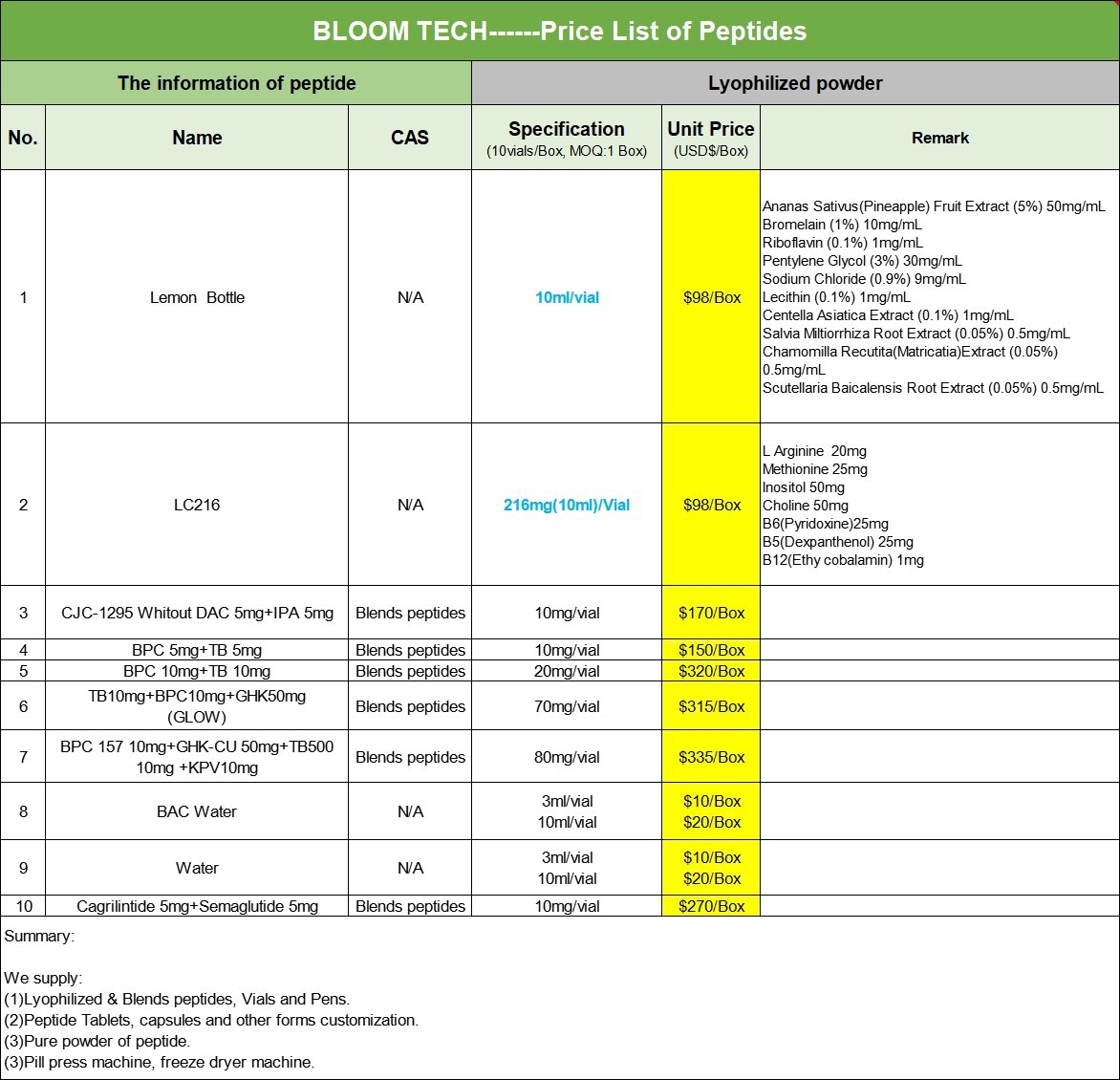

Leuproreline-acetaat COA



Centrale vroegtijdige puberteit (CPP) is een veel voorkomende endocriene stoornis bij kinderen, gedefinieerd als het begin van secundaire geslachtskenmerken vóór de leeftijd van 8 jaar bij meisjes en 9 jaar bij jongens, veroorzaakt door de voortijdige activering van de hypothalamus-hypofyse- gonadale (HPG)-as. Zonder tijdige interventie kan dit leiden tot een korte volwassen lengte, een onevenwichtige psychologische ontwikkeling en andere complicaties. Als een injecteerbare suspensie met langdurige-werkende-afgifte,Leuproreline-acetaatsuspensiemaakt gebruik van de unieke voordelen van zijn microdeeltjesverspreidingssysteem om de functie van de gonadale as nauwkeurig te reguleren, en ontpopt zich als een eerste-klinisch medicijn voor de behandeling van centrale vroegtijdige puberteit. Het biedt een veilige en zeer effectieve therapeutische optie voor pediatrische patiënten, waarbij een stabiele werkzaamheid in evenwicht wordt gebracht met een goede medicatieverdraagbaarheid voor kinderen.
Nauwkeurige remming van de gonadale as, gemedieerd door de suspensieformulering
Het kernmechanisme ervan bij de behandeling van centrale vroegtijdige puberteit is gebaseerd op de synergetische voordelen van de hoge- krachtige LH-RH-derivaateigenschappen en de suspensieformulering, waardoor bidirectionele regulatie en lang-werkende remming van de HPG-as mogelijk is. Als synthetische gonadotropine-releasing hormoon (GnRH)-agonist heeft het actieve ingrediënt een veel hogere affiniteit voor GnRH-receptoren in de hypofyse dan endogeen GnRH en vertoont het een sterkere weerstand tegen proteolytische enzymen. De suspensieformulering suspendeert het medicijn, door middel van microdeeltjesdispersietechnologie, gelijkmatig in een oplosmiddel; na injectie lost het langzaam op en komt het medicijn vrij in onderhuids of spierweefsel, waardoor abrupte stijgingen en dalingen van de medicijnconcentratie in het bloed worden voorkomen.
In de beginfase van de toediening treedt een voorbijgaande ‘opvlammingsreactie’ op, die de hypofyse kortstondig stimuleert om luteïniserend hormoon (LH) en follikel-stimulerend hormoon (FSH) af te scheiden, wat leidt tot een tijdelijke verhoging van de geslachtshormoonspiegels. Dit kan bij sommige pediatrische patiënten een lichte verergering van de secundaire geslachtskenmerken veroorzaken, maar de reactie is van korte- duur en verdwijnt spontaan als de medicatie wordt voortgezet. Bij langdurige toediening zorgt de eigenschap voor langdurige afgifte van de suspensieformulering ervoor dat de geneesmiddelconcentratie in het bloed stabiel blijft en remt de gevoeligheid van de GnRH-receptoren in de hypofyse door middel van negatieve feedbackregulatie. Dit vermindert de secretie van LH en FSH aanzienlijk tot pre- puberale niveaus, waardoor de reactie van de eierstokken of teelballen op gonadotropines wordt geremd, de concentraties estradiol en testosteron worden verlaagd, de progressie van secundaire geslachtskenmerken wordt geblokkeerd en de snelheid van botleeftijdssluiting wordt vertraagd om tijd te winnen voor lengtegroei.
Vergeleken met conventionele injecties kan de suspensieformulering de snelheid van de geneesmiddelafgifte nauwkeurig regelen, waardoor herhaling van de behandeling als gevolg van schommelingen in de geneesmiddelconcentratie wordt vermeden, en is daarom geschikter voor behandelingsbehoeften op de lange- termijn.
Dubbele voordelen van symptoombeheersing en behoud van groeipotentieel
Klinische studies hebben dat bevestigdLeuproreline-acetaatsuspensieheeft definitieve werkzaamheid bij de behandeling van centrale vroegtijdige puberteit, waarbij de meerdere doelen van secundaire controle van de geslachtskenmerken, vertraging van de botleeftijd en behoud van lengte worden bereikt, waarbij de werkzaamheid niet wordt beïnvloed door de body mass index (BMI) van de patiënt. Wat de controle van de secundaire geslachtskenmerken betreft, vertraagt de progressie van de secundaire geslachtskenmerken bij de meeste pediatrische patiënten aanzienlijk na 1-2 behandelingscycli: de borstontwikkeling stagneert en het vaginale bloeden stopt bij meisjes, terwijl de vergroting van de testis en de groei van het schaamhaar bij jongens worden geremd. Na een jaar behandeling zijn bij meisjes het volume van de eierstokken en de baarmoeder, evenals de follikeldiameter, aanzienlijk verminderd en stabiliseren de geslachtshormoonspiegels zich op pre-puberale niveaus.
In termen van lengtebehoud vertraagt het lang-werkende remmende effect van de suspensieformulering effectief de sluiting van de botleeftijd, waardoor kostbare tijd wordt gewonnen voor lengtegroei. Uit een Zuid-Koreaans cohortonderzoek bleek dat meisjes die vóór de leeftijd van 8 jaar met de behandeling begonnen, een voorspelde lengtetoename van 1,5 centimeter hadden na 1 jaar medicatie, met een significante afname van de snelheid waarmee de botten verouderen. De menarche werd op natuurlijke wijze hervat bij patiënten 0,9-1,5 jaar na het staken van de medicatie, met een gemiddelde leeftijd waarop de behandeling werd hervat van 12,6-13,6 jaar, wat consistent is met het normale patroon van de puberale ontwikkeling. Bovendien worden de markers van het botmetabolisme in het serum (amino-terminaal propeptide van type I procollageen, -crosslaps, enz.) aanzienlijk verminderd na de behandeling, waardoor de snelheid van het botmetabolisme wordt vertraagd, wat het remmende effect ervan op de progressie van de botleeftijd verder bevestigt en een garantie biedt voor de verbetering van de uiteindelijke volwassen lengte.

Nauwkeurige controle van de bereiding van polypeptiden

De synthese vanLeuproreline-acetaatsuspensieactief farmaceutisch ingrediënt (API) is voornamelijk gebaseerd op de vaste-fasesynthesemethode, waarbij de kern de stapsgewijze koppeling van aminozuren is om een nonapeptidestructuur te construeren. Nauwkeurige controle wordt gedurende het hele proces geïmplementeerd om een hoge zuiverheid en biologische activiteit te garanderen. Er wordt gebruik gemaakt van de Fmoc- of Boc-beschermingsstrategie, met polystyreenhars als de vaste-fasedrager, en aminozuren worden opeenvolgend gekoppeld vanaf het C--uiteinde. Na elke koppelingsstap wordt de reactie-efficiëntie geverifieerd door middel van professionele tests om de vorming van bijproducten zoals deletiepeptiden strikt te voorkomen. Het ruwe peptide ondergaat meer-trapszuivering via omgekeerde-fase hoge-vloeistofchromatografie met hoge-prestaties (RP-HPLC) om onzuiverheden en resterende reactanten volledig te verwijderen, gevolgd door zoutomzetting via ionenuitwisseling om het acetaatzout te vormen.
Deze stap verbetert niet alleen de vetoplosbaarheid van het medicijn, maar verbetert ook de chemische stabiliteit ervan, waardoor een solide basis wordt gelegd voor de daaropvolgende bereiding van de doseringsvorm. De zuiverheid van het gezuiverde API moet meer dan 99% bedragen en het gehalte aan acetaationen moet strikt worden gecontroleerd binnen het gespecificeerde bereik om een consistente werkzaamheid van het geneesmiddel over batches te garanderen. Ten slotte wordt het API onderworpen aan steriele filtratie en vriesdrogen om een los API in poedervorm te vormen, dat niet alleen de daaropvolgende bereiding van microbolletjes vergemakkelijkt, maar ook de biologische activiteit maximaal behoudt en de afbraak van polypeptidemoleculen voorkomt.
Kerngarantie voor lang-werkende aanhoudende vrijgave
De langwerkende -aanhoudende- afgifte-eigenschap van de suspensie is afhankelijk van de nauwkeurige bereiding van PLGA-microsferen en de constructie van het suspensiesysteem, waarbij de kern bestaat uit de implementatie van het laden van geneesmiddelen via de emulgerings-oplosmiddelverdampingsmethode. Het product, PLGA, gelatine en andere grondstoffen worden opgelost in dichloormethaan om een organische fase te vormen, die vervolgens wordt toegevoegd aan een waterige fase die een oppervlakteactieve stof bevat. Emulgering op hoge-snelheid wordt uitgevoerd om een O/W-emulsie te vormen, en PLGA wordt gestold om microsferen te vormen door langzame verdamping van het oplosmiddel. De deeltjesgrootte van de microsferen wordt strikt gecontroleerd binnen het bereik van 1-10 μm, waardoor de uniformiteit van de suspensie wordt gegarandeerd en tegelijkertijd een stabiele geneesmiddelafgifte wordt bereikt. Na wassen en vriesdrogen-worden de microbolletjes gemengd met mannitol om het poeder te vormen in de voorste kamer van een injectiespuit met twee kamers; het verdunningsmiddel in de achterste kamer wordt bereid door natriumcarboxymethylcellulose, polysorbaat 80, azijnzuur en andere componenten zorgvuldig te doseren, en de pH van het systeem wordt aangepast op 4,0-6,0.
Dit handhaaft niet alleen de stabiliteit van de suspensie, voorkomt aggregatie en sedimentatie van microbolletjes, maar vermindert ook irritatie van lokale weefsels tijdens injectie. Ten slotte worden het poeder en het verdunningsmiddel afzonderlijk in spuiten met dubbele- kamer gevuld met behulp van een aseptisch proces, en wordt de sterilisatie voltooid na het verzegelen. Tijdens gebruik kunnen ze snel worden gemengd tot een uniforme suspensie, waardoor niet alleen het risico op besmetting wordt vermeden, maar ook een nauwkeurige en foutloze dosering- wordt gegarandeerd.
Volledige-proceskwaliteitscontrole

Tijdens het productieproces moet een volledig-proceskwaliteitscontrolesysteem worden opgezet, waarbij multi-multidimensionale tests worden uitgevoerd van grondstoffen tot eindproducten om de veiligheid, werkzaamheid en stabiliteit van het product te garanderen. In de API-fase zijn de belangrijkste monitoringindicatoren de zuiverheid en het gehalte aan acetaationen: de zuiverheid mag niet minder zijn dan 99% en het gehalte aan acetaationen moet voldoen aan gevestigde normen om een stabiele basis voor de werkzaamheid van geneesmiddelen te garanderen. In de voorbereidingsfase van de microbolletjes zijn de belangrijkste controle-indicatoren de verdeling van de deeltjesgrootte en de belading van het geneesmiddel: de deeltjesgrootte moet strikt op 1-10 μm worden gehouden en de afwijking van de belading van het geneesmiddel moet binnen ± 5% worden gecontroleerd, wat direct de daaropvolgende geneesmiddelafgiftesnelheid bepaalt. Voor de afgewerkteLeuproreline-acetaatsuspensieDe pH-waarde en de stabiliteit van de microdeeltjes worden getest: de pH-waarde moet stabiel zijn op 4,0-6,0 en er treedt geen duidelijke sedimentatie op binnen 30 minuten na reconstitutie, waardoor een uniforme distributie van het geneesmiddel na toediening wordt gegarandeerd.
Aseptische en veiligheidsindicatoren zijn zelfs nog belangrijker: het bacteriële endotoxinegehalte moet lager zijn dan 0,5 EU/ml, en de steriliteitstest moet volledig gekwalificeerd zijn om het risico op infectie te elimineren. Bovendien moeten het molecuulgewicht van PLGA en de geneesmiddelafgiftesnelheid van de microsferen gelijktijdig worden gecontroleerd om een stabiele geneesmiddelafgifte gedurende de behandelingscyclus van 4- weken te garanderen, waarbij de schommelingen in de geneesmiddelconcentratie in het bloed niet groter zijn dan 20%, wat geschikt is voor de langetermijnbehandelingsbehoeften van pediatrische patiënten.
Zorgen voor langdurige-acteerstabiliteit
Verpakkings- en opslagomstandigheden zijn rechtstreeks van invloed op de houdbaarheid en gebruiksveiligheid van het product, en strikte naleving van professionele specificaties is vereist. Het product is verpakt in voorgevulde spuiten met twee-kamers, gemaakt van licht-materiaal, die de oxidatieve schade aan het medicijn, veroorzaakt door licht, effectief blokkeren; het afdichtingssysteem maakt gebruik van materialen met een hoge-barrière om de infiltratie van lucht en vocht te voorkomen, waardoor vochtabsorptie en aankoeking van microbolletjes wordt vermeden. Ondertussen wordt een speciaal verdunningsmiddel meegeleverd om onmiddellijke injectie na het mengen te garanderen. Opslag moet plaatsvinden in een licht-dichte omgeving onder de 25 graden, en bevriezingsopslag is ten strengste verboden, omdat bevriezing de microsfeerstructuur zal beschadigen en verlies van de aanhoudende- afgiftefunctie zal veroorzaken; Hevig schudden moet tijdens transport worden vermeden om veranderingen in de deeltjesgrootte van de microbolletjes te voorkomen die de werkzaamheid van het geneesmiddel kunnen beïnvloeden.

De houdbaarheid van ongeopende producten is 24 maanden en de injectie moet onmiddellijk na reconstitutie worden uitgevoerd; langdurige opslag is ten strengste verboden om afbraak van het geneesmiddel of instabiliteit van het ophangsysteem te voorkomen. Het etiket moet duidelijk de dosering, de houdbaarheid, de reconstitutiemethode en de voorzorgsmaatregelen voor gebruik vermelden, waardoor duidelijke richtlijnen worden gegeven voor een correcte klinische werking en het voorkomen van medicatiefouten.
Veelgestelde vragen
1. Wat is het product?
(LOO-proh-lide A-seh-tayt)Een medicijn dat wordt gebruikt onder de merknamen Eligard en Lupron Depot om prostaatkanker te behandelenen onder de merknaam Lupron Depot om problemen met het endometrium (slijmvlies van de baarmoeder) en baarmoederfibromen (goedaardige gezwellen van de baarmoeder) te behandelen.
2. Hoe lang duurt het voordat het werkt?
Klinische onderzoeken met het product hebben aangetoond dat de testosteronspiegels tijdens de eerste vier dagen van de behandeling toenamen bij de meerderheid van de patiënten die niet-georchidectomeerd waren. Vervolgens daalden ze en bereikten ze het castratieniveau2-4 weken. Eenmaal bereikt, bleven de castratieniveaus gehandhaafd zolang de medicamenteuze behandeling werd voortgezet.
3.Is het product een chemotherapiemedicijn?
Het isgeen chemotherapiebehandeling, maar een hormoongeneesmiddel op recept dat wordt gebruikt bij de palliatieve behandeling van gevorderde prostaatkanker. Palliatieve behandeling wordt gebruikt om pijn of andere symptomen te verlichten en de kwaliteit van uw leven te verbeteren.
4. Wat moet ik vermijden tijdens het gebruik van het product?
Gebruik dit medicijn niet met een van de volgende zaken:
Kuisbes.
Cisapride.
Dronedarone.
Pimozide.
Thioridazine.
Populaire tags: leuprolide-acetaatsuspensie, China leuprolide-acetaatsuspensie fabrikanten, leveranciers
















